海军军医大学药学系盛春泉教授团队与复旦大学鲁伯埙教授团队合作取得重大科研突破。3月19日,双方合作的研究成果荣登国际顶级期刊《Cell》(影响因子:42.5)。盛春泉教授为共同通讯作者,药学系青年文职科研骨干王蔚博士为共同第一作者,该团队主导了本研究的药物化学核心工作。

△该成果3月19日在Cell在线发表
研究背景
靶向蛋白降解是当前药物研发的重要前沿方向。其中,蛋白水解靶向嵌合体(PROTAC)作为主流技术之一,可高效降解多种胞质及核内疾病相关蛋白,然而在作用于膜蛋白方面仍存在明显局限。

△药学系主任盛春泉教授在实验室工作

△药学系王蔚博士在实验室工作
近年来,针对膜蛋白的降解技术主要依赖以抗体为基础的大分子溶酶体靶向平台。这类方法虽具备一定可行性,但普遍存在制备工艺复杂、分子体积较大、体内稳定性不足以及降解效率不理想等问题,严重制约其成药潜力与临床转化前景。因此,亟需开发新型膜蛋白降解策略,以突破当前技术瓶颈,拓展其在创新药物研发中的应用空间。
研究亮点
针对上述技术瓶颈,本研究将目光投向另一条长期被忽视的细胞内质量控制系统——内质网相关降解(ERAD)通路,并在此基础上发展了一种靶向该通路的小分子降解策略,命名为ERADEC(ERAD-engaging chimeras)。该策略通过特异性招募定位于内质网的E3泛素连接酶SYVN1,识别并泛素化在内质网折叠完成的跨膜蛋白,进而经由ERAD途径将其引导降解。这一机制为膜蛋白靶点的干预提供了全新思路和技术路径。
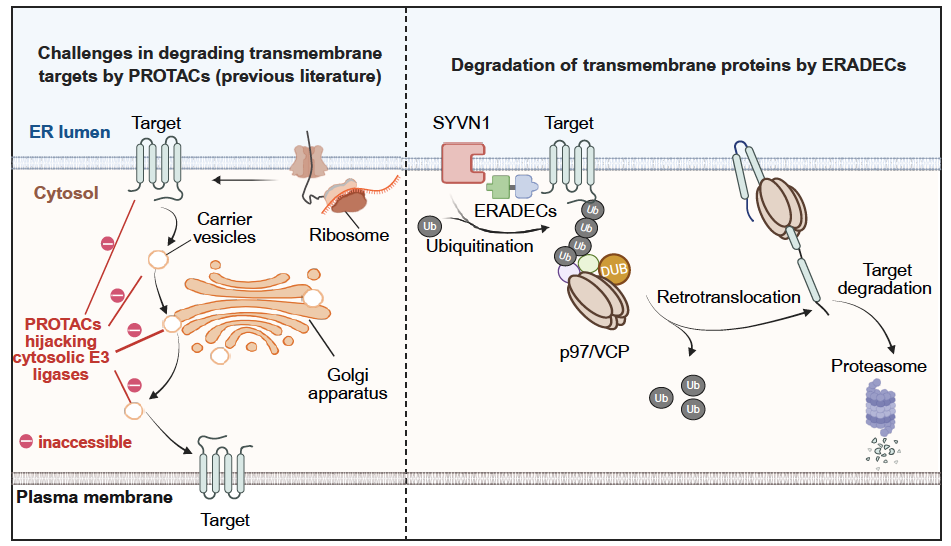
△传统 PROTACs 与新型 ERADECs 的降解机制对比
研究发现,desonide可作为靶向E3连接酶SYVN1的有效配体。基于此,研究团队以膜蛋白PD-L1为模型靶点开展概念验证,合理设计并合成了一系列ERADEC降解剂(命名为P-ERADECs)。这些分子一端结合SYVN1,另一端识别目标蛋白,中间由化学连接子相连。实验结果表明,大多数P-ERADEC降解剂在亚纳摩尔(sub-nM)浓度下即可高效诱导PD-L1蛋白降解。
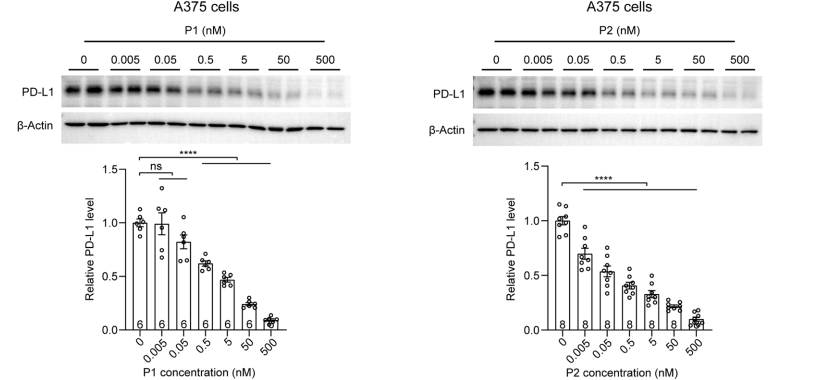
△代表化合物的体外降解活性
进一步研究表明,P-ERADECs的降解功能依赖SYVN1和ERAD途径。
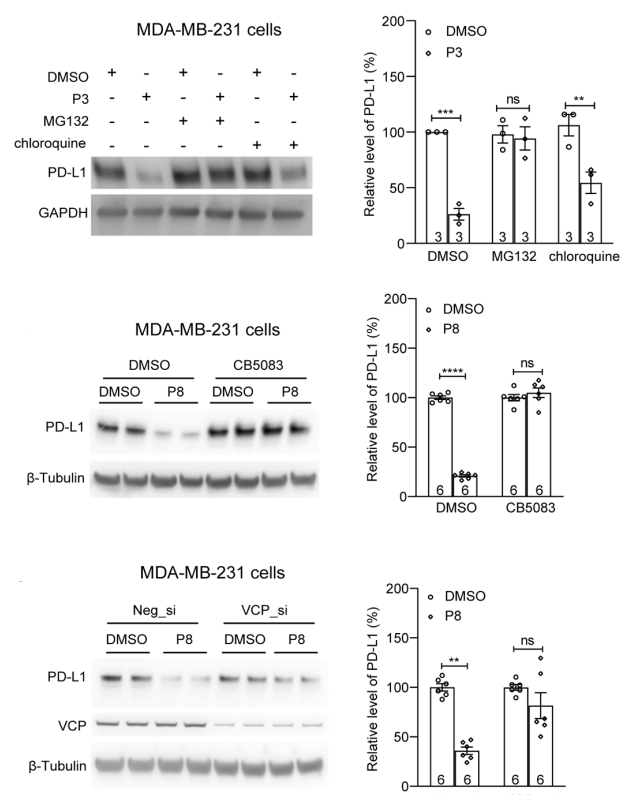
△P-ERADECs的降解功能依赖ERAD途径
P-ERADECs能高效介导PD-L1与SYVN1形成三元复合物,这是其发挥降解功能的结构基础。
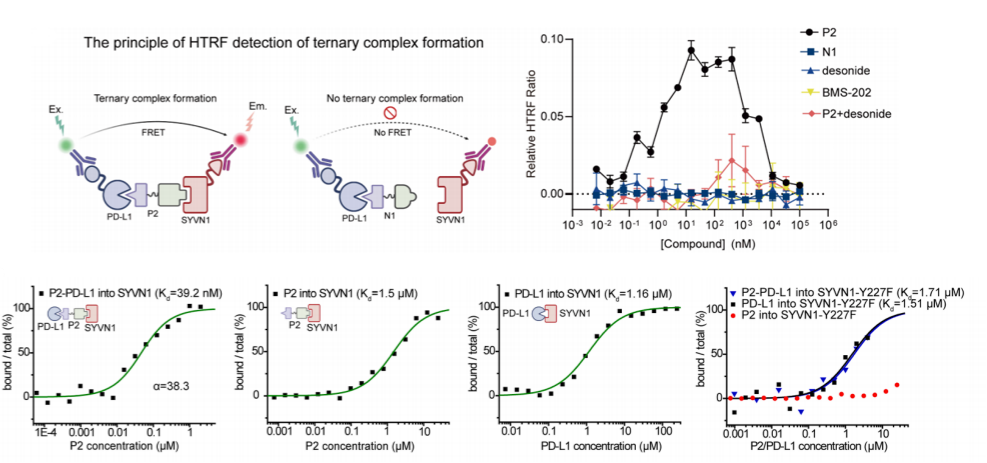
△P-ERADECs高效诱导PD-L1-P-ERADEC-SYVN1三元复合物的形成
代表性化合物在小鼠体内展现出显著的抗肿瘤疗效,伴随肿瘤组织中PD-L1蛋白的显著下调及T细胞浸润增强。
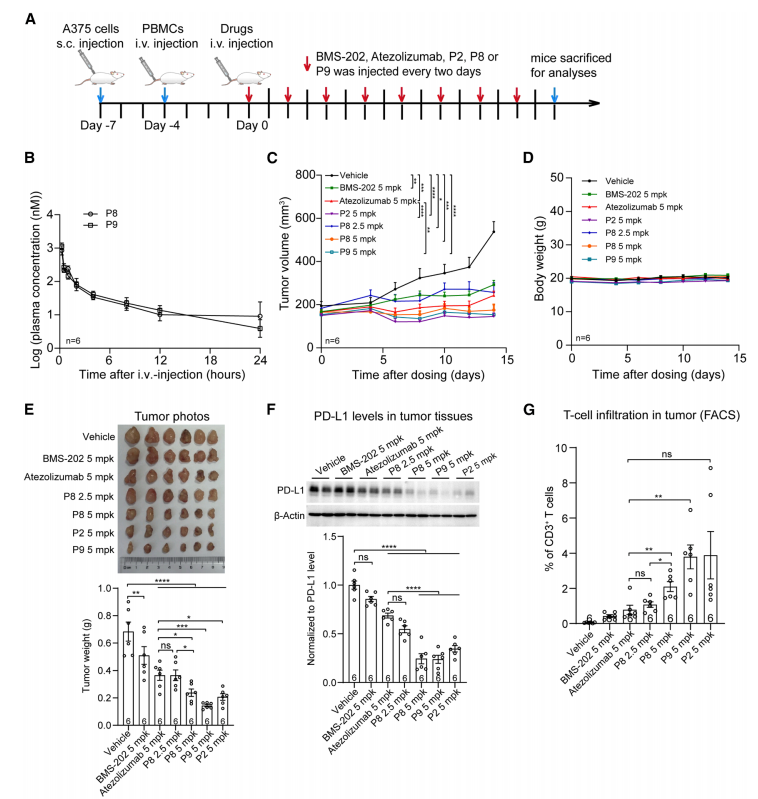
△P-ERADECs的体内抗肿瘤活性
重要意义:本研究首次系统性地利用内质网质量控制体系,发展了一种靶向跨膜蛋白降解的全新策略,为突破传统降解技术的应用局限提供了变革性工具,有望为更多原本难触及的靶点提供有效降解途径。
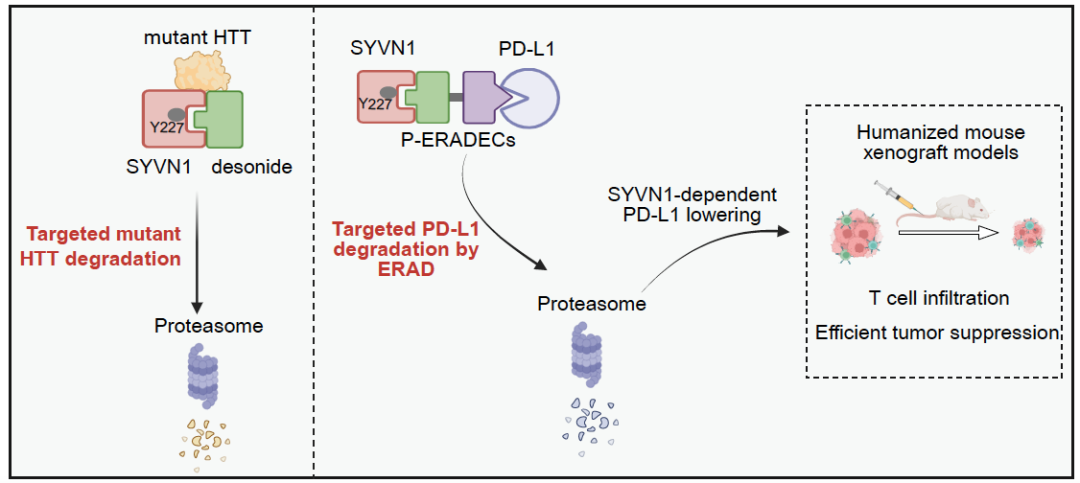
△PERADECs 在特定疾病靶点上的应用实例
研究团队
鲁伯埙、盛春泉教授为论文通讯作者,宋海坤、王蔚、梅婷芳、郑惠文为论文的共同第一作者。服部素之、刘瑞、丁滪、费义艳,及曹禹等也为该研究作出了重要贡献。
其中,药学系青年文职科研骨干王蔚博士作为近年新入职的社招文职人员,充分展现了快速融入军队科研体系并取得突破性进展的潜力。

共同第一作者:王蔚
专家简介:博士,毕业于中国科学院上海药物所,在海军军医大学完成博士后研究工作后留校任教,现任药学系讲师。近年来聚焦于新型靶向蛋白降解技术研究,相关成果以第一(含共同)作者发表于Cell、Advanced Drug Delivery Reviews、Journal of Medicinal Chemistry等国际权威期刊,参编学术专著《靶向蛋白降解》。主持完成国家自然科学基金青年项目(C类)1项,入选药学系“时珍学者”培育计划。

共同通讯作者:盛春泉
专家简介:海军军医大学药学系主任,教授、博士生导师。国家杰出青年基金获得者。主编出版中英文学术专著5部。在Cell、Nature Communications等国际权威期刊发表SCI论文200余篇,获得国家发明专利授权30余项。获中国科协“求是”杰出青年科学奖、国家科技进步二等奖、中国药学会科学技术奖一等奖等重要奖项。主要从事靶向蛋白降解和抗真菌药物研究。

主 办:政治工作处
刊 期:总第1717期
监 制:张 波
主 编:李晋宇
编 辑:王泽锋 李也
来 源:药学系
投稿邮箱:hydfbwx@163.com


 高招云直播
高招云直播




